Så landade avtalet om EU:s nya läkemedelslag – ministern lättad
Andreas Wind
Journalist och redakör Altinget Hälsa
Linda Berglund
Redaktör Altinget Vård och Hälsa samt Altinget Omsorg
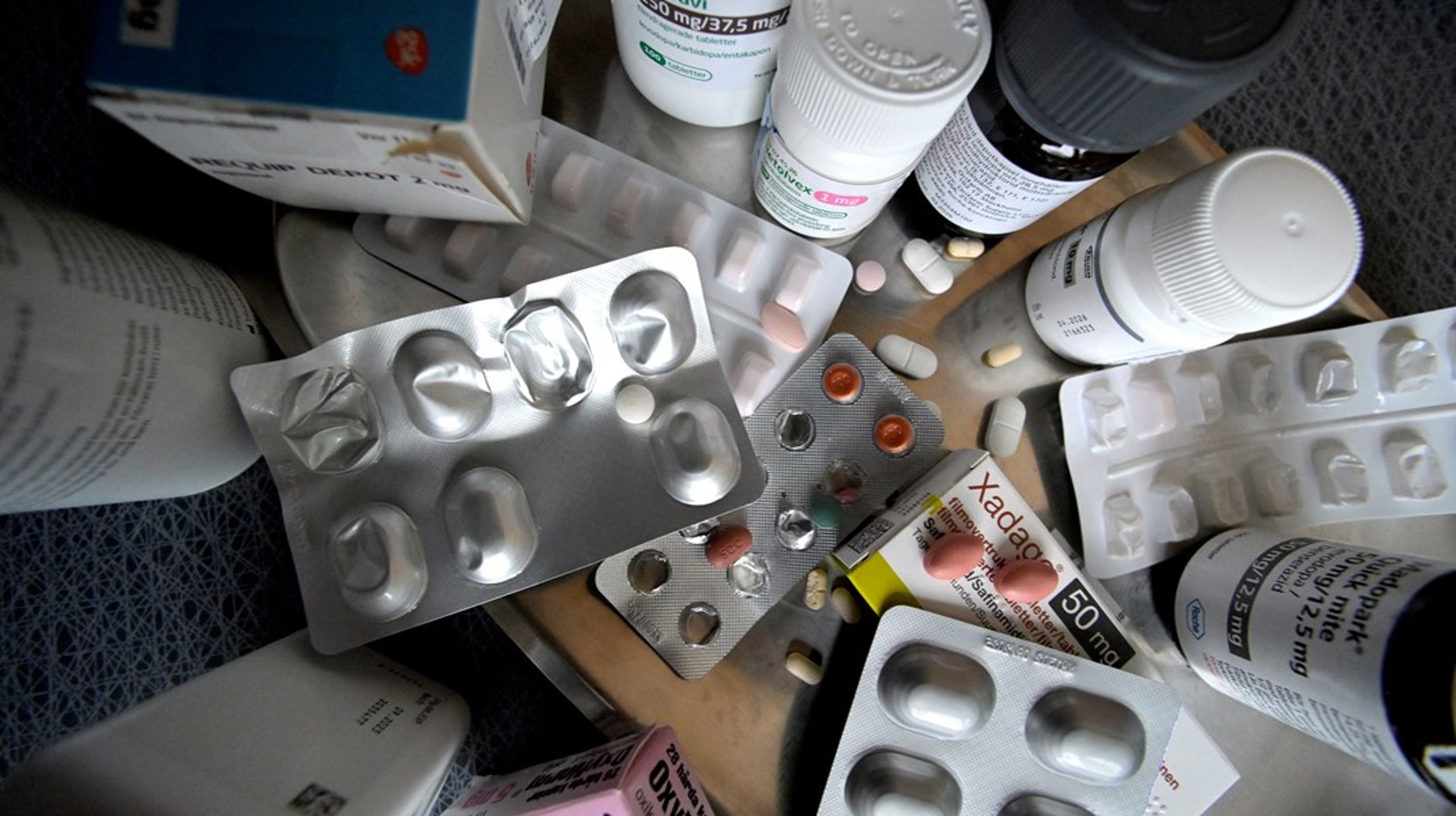
Det har varit på väg i åratal, men nu är parlamentet och ministerrådet överens om EU:s nya läkemedelspaket, som är en reform av hela regleringen av den europeiska läkemedelsindustrin.
Det var den danska hälso- och inrikesministern Sophie Løhde (Venstre) som kommenterade avtalet, som landade natten till torsdag.
Hon kallar avtalet ett viktigt steg i europeisk hälsopolitik:
”Läkemedelspaketet är till gagn för miljoner européer och stärker Europas förmåga att utveckla framtidens läkemedel”, säger hon i ett pressmeddelande.
Även parlamentets chefsförhandlare, spanska Dolors Montserrat från högergruppen EPP, är nöjd med resultatet.
”Detta avtal sänder en tydlig och kraftfull signal: Patienterna står i centrum för vårt arbete, och vi har lyckats samla alla politiska krafter i Europaparlamentet bakom att arbeta för bättre tillgång till medicin – genom att säkra innovation, främja utvecklingen av mer effektiva behandlingar och skapa mer överkomliga alternativ för alla medborgare”, säger hon.
Regulatoriskt skydd av innovation
- Dataskydd: 8 år med ensamrätt att använda egna prekliniska och kliniska data.
- Marknadsskydd (grundperiod): 1 år med exklusiv försäljning utan omedelbar konkurrens från generika/biosimilarer.
- Tak för regulatoriskt skydd: 11 år.
- Möjliga tillägg på 12 månader vid flera kriterier:
- Om produkten adresserar ett otillgodosett medicinskt behov.
- Vid nytt aktivt ämne och uppfyllda krav om bl.a. jämförande kliniska studier och studier i flera medlemsstater.
- Vid nya terapeutiska indikationer med betydande klinisk fördel jämfört med befintlig behandling.
- Särläkemedel: “Breakthrough”-produkter (utan aktuell behandling) kan få upp till 11 års marknadsexklusivitet.
Bekämpning av antimikrobiell resistens (AMR)
- Överförbar exklusivitetsvoucher på 12 månaders extra dataskydd till en annan godkänd produkt efter företagets val.
- “Blockbuster”-klausul: Kan inte användas på produkter med årlig bruttoförsäljning över 490 miljoner euro de fyra föregående åren.
- Strängare krav: bl.a. obligatoriskt recept för all antibiotika.
Tillgång till medicin och generika
- Bolar-undantaget förtydligas: Gör det lättare för generika-/biosimilarproducenter att genomföra nödvändiga studier och lämna in ansökningar under patenttiden, så att billigare alternativ kan vara redo vid utgången.
- Försörjningskrav (artikel 56a): Medlemsstater kan kräva att företag levererar tillräckliga mängder för att täcka patienternas behov – med skydd mot missbruk för parallellhandel.
- Förebyggande planer: Företag måste utarbeta och uppdatera planer för att förebygga brist på receptbelagda läkemedel.
Regelförenkling
EMA-procedurer optimeras:
- Snabbare behandling av ansökningar om marknadsföringstillstånd.'
- Obegränsad giltighet: Marknadsföringstillstånd blir som utgångspunkt tidsobegränsade.
- Regulatory sandboxes: Möjlighet för försöksordningar där nya och innovativa behandlingar kan utvecklas och testas under kontrollerade ramar.
Socialminister Jakob Forssmed kallar avtalet det viktigaste som hänt inom läkemedelsområdet på 20 år. Med det nya läkemedelspaketet landar den så kallade dataskyddsperioden på åtta år, vilket Sverige drivit i förhandlingarna.
– Det känns oerhört bra, särskilt i den nya miljön vi befinner oss i där den här typen av saker spelar stor roll för var bolag bestämmer sig för att etablera sig och utveckla läkemedel och så vidare. Det här spelar en jättestor roll för europeisk konkurrenskraft och det spelar en stor roll för Sverige, säger han.
Däremot gick inte tidgränsen för marknadskyddet Sveriges väg.
Företagen får ett år med marknadsskydd. Det är perioder där företagen har ensamrätt att utveckla och sälja det nya läkemedlet innan konkurrenter kan kopiera medicinen och därmed pressa priset.
Företagen kan med avtalet maximalt få elva års skydd genom en rad incitament och just frågan om skyddsperioden har varit den mest omdiskuterade i förhandlingarna.
Näringsvänligt kompromissförslag
Det väckte både uppmärksamhet och oro när kommissionen i april lade fram sitt förslag, där de föreslog att förkorta skyddsperioden drastiskt för att pressa ner priset på ny medicin, så att alla europeiska länder skulle ha råd med den bästa medicinen i framtiden.
Men förslaget stämplades snabbt som näringsfientligt, och både parlamentet och ministerrådet har – var för sig, och nu även tillsammans – kommit fram till ett mer näringsvänligt kompromissförslag.
Danska Stine Bosse (Moderaterne) är därför också nöjd med resultatet:
"Om inte life science-sektorn ska gå samma väg som tech-sektorn, som flyttade till USA, måste vi agera nu. Europa ska vara en attraktiv plats att utveckla framtidens medicin. Europa ska vara en plats där företag har rätt förutsättningar att investera och stanna – så att vi kan säkra både innovation, jobb och tillgång till bra och billig medicin för våra patienter", säger hon i ett pressmeddelande.
Behöver landa
Jakob Forssmed säger att Sverige hade velat se ett betydligt mer omfattande marknadsskydd, men att helheten är viktigare.
– Givet att vi fick vouchern på plats och det incitamentet som också då ger drivkrafter för nya antibiotika och samtidigt kan medföra att en del företag då kan köpa extra marknadsskydd så tycker jag att det här är bra, totalt sett.
Att förhandlingarna kunde slutföras är också viktigt i förhållande till handelspolitiska besked från inte minst USA.
– Det är inte så att det finns ett överflöd av tid här utan vi behöver få det här på plats. Det ger mer moderna förutsättningar. Det ger mer förutsägbarhet för bolagen kring vad som gäller. Och förutsägbarhet i en oförutsägbar värld skulle jag säga har ett väldigt stort värde, säger Jakob Forssmed.
Det preliminära avtalet måste nu godkännas av både Europeiska unionens råd och Europaparlamentet innan det formellt antas och träder i kraft efter offentliggörandet i EU:s officiella tidning.
Artikeln är en bearbetad översättning från Altinget.dk